| ボルタ電池 | ダニエル電池 | |
 |
 |
|
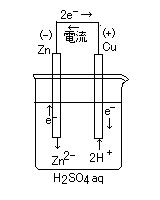
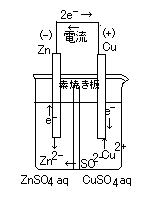
| (-) Zn | H2SO4 aq | Cu (+) | (-) Zn | ZnSO4 aq || CuSO4 aq | Cu (+) | |
| 負極 | Zn → Zn2+ + 2e- | Zn → Zn2+ + 2e- |
| 正極 | 2H+ + 2e- → H2 | Cu2+ + 2e- → Cu |
| マンガン電池 (ルクランシェ電池) | 鉛蓄電池 | |
 |
 |
|
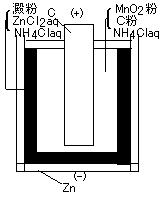
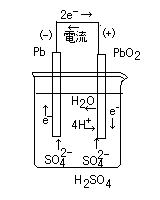
| (-) Zn | NH4Claq | MnO2, C (+) | (-) Pb | H2SO4aq | PbO2 (+) | |
| 負極 | Zn + 4NH4+ → [Zn(NH3)4]2+ + 2e- | Pb + SO42- → PbSO4 + 2e- |
| 正極 | 2MnO2 + 2H+ + 2e- → Mn2O3 + H2O | PbO2 + 4H+ + SO42- + 2e- → PbSO4 + 2H2O |
| アルカリ蓄電池 | ||
| (-) Cd | KOHaq | NiO(OH) (+) | ||
| 負極 | Cd + 2OH- → Cd(OH)2 + 2e- | |
| 正極 | 2NiO(OH) + 2H2O + 2e- → 2Ni(OH)2 + 2OH- |